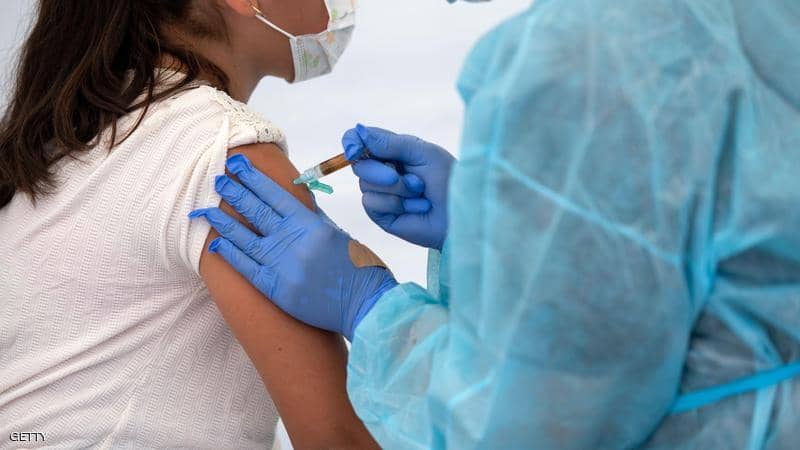
تصميم اللقاحات بشكل أسرع : إن تحليل جميع أجزاء الجهاز المناعي في وقت واحد بعد التطعيم من شأنه تسريع تطوير لقاحات فعالة ، وتوجيه ضربة قاتلة لفيروس الإيدز.
كان علماء الأحياء الذين يعملون في مجال الإيدز يأملون في أن يكون اللقاح الذي طورته معامل ميرك والمعهد الأمريكي لدراسة الحساسية والأمراض المعدية هو اللقاح الذي طال انتظاره لمدة 30 عامًا. تحطمت هذه الآمال في عام 2007 ، عندما كشفت نتائج تجربة سريرية شملت 3000 شخص أن اللقاح غير فعال. لم يقتصر الأمر على أن تلقيح اللقاح لم يحمي المشاركين في التجربة السريرية ، بل زاد أيضًا من خطر الإصابة بفيروس نقص المناعة البشرية بالنسبة لبعضهم.. تم تخصيص ملايين الدولارات وأكثر من عشر سنوات من البحث لتطوير هذا اللقاح. خلال نفس الفترة ، مات 18 مليون شخص بسبب الإيدز وأصيب ملايين آخرون.
في الواقع ، حتى اليوم ، بعد عقود من البحث ، لم يتضح بعد كيفية تطوير لقاح فعال ضد فيروس نقص المناعة البشرية . بالتأكيد ، حققت بعض اللقاحات ، مثل تلك المستخدمة ضد شلل الأطفال أو الجدري ، نجاحًا باهرًا. لكن في الواقع ، لعب الحظ دورًا كبيرًا في نجاحهم. بناءً على معرفتهم المحدودة بجهاز المناعة ومسببات الأمراض ، علماء الأحياء
جدول المحتويات
لقد ابتكرت بالفعل لقاحات أثبتت ، بعد تعديلات قليلة ، أنها فعالة في حماية الأشخاص من هذه العدوى
لقد ابتكرت بالفعل لقاحات أثبتت ، بعد تعديلات قليلة ، أنها فعالة في حماية الأشخاص من هذه العدوى. ولكن في كثير من الأحيان ، عندما لا يعرف المرء أي تفاعلات مناعية تحمي حقًا ، تكون النتائج مخيبة للآمال ، خاصةً عندما لا يرى المرء عدم الفعالية إلا بعد تجربة سريرية كبيرة.
إقرأ أيضا:تراجع القوى الأوروبيةومن هنا يأتي السؤال الذي يطرحه علماء المناعة على أنفسهم: كيف نطور لقاحات فعالة وتسريع تقييمها؟ لتحقيق ذلك ، سيكون من الضروري أن نفهم بدقة جميع ردود الفعل المناعية التي يسببها لقاح فعال حقًا. سيكون من الضروري ، على سبيل المثال ، اكتشاف الخلايا المناعية المتورطة وكيفية تفاعلها ، أو حتى الجينات التي يتم تنشيطها أو تثبيطها بواسطة هذه الخلايا. يمكن لعلماء المناعة بعد ذلك تجميع هذه المعلومات معًا لتوضيح الاستجابة المناعية الوقائية حقًا. يمكن استخدام هذا الملف الشخصي لتحديد مكونات لقاح وقائي ضد المرض.
تصميم اللقاحات بشكل أسرع : مقارنة مئات الصيغ الممكنة
من خلال مقارنة مئات الصيغ الممكنة ، سيختار علماء الأحياء تلك التي تنتج ملفًا مناعيًا قريبًا من المظهر الجانبي النموذجي. ثم يقومون بتحسين هذه التركيبات من خلال إجراء تجارب سريرية سريعة وصغيرة الحجم ، حتى يحصلوا على اللقاحات التي تؤدي إلى التواقيع البيولوجية المثلى. من خلال الاقتراب من التوقيع المثالي ، سيعرفون بسرعة ما إذا كان من المحتمل أن يكون اللقاح فعالاً. وهكذا ، حتى قبل اختبار اللقاح التجريبي في تجارب سريرية واسعة النطاق ، سنكون متأكدين تقريبًا من نجاحه.
لم يكن لدى علماء الأحياء المعرفة ولا الأدوات لتحقيق هذا الهدف
حتى الآن ، لم يكن لدى علماء الأحياء المعرفة ولا الأدوات لتحقيق هذا الهدف. تطلب الأمر فرقًا متعددة التخصصات من علماء المناعة وعلماء الأحياء الدقيقة القادرين على نمذجة الأنظمة البيولوجية المعقدة وتحديد خصائصها بين كميات كبيرة من البيانات. لقد احتجنا أيضًا إلى أدوات تقيس التغييرات في نشاط الجينات ، وكميات البروتين المنتجة ، وسلوك الخلية ، والعديد من المعلمات المحددة للاستجابات المناعية في وقت واحد وبشكل متكرر – ناهيك عن أجهزة الكمبيوتر القوية والبرامج القادرة على معالجة جميع هذه البيانات. اليوم، تعمل الفرق العاملة في مجال ما يسمى ببيولوجيا الأنظمة على تطوير أدوات من شأنها تحسين طريقة تصميم اللقاحات. وهكذا يبدأ المجتمع العلمي في اكتشاف تفاصيل ردود الفعل المناعية اللازمة لحماية الشخص منفيروس نقص المناعة البشرية . يستخدم هذا النهج اليوم لتطوير لقاحات ضد الإيدز والسل والملاريا والأنفلونزا.
إقرأ أيضا:من هو لويس الثامن عشر ملك التسوية؟تصميم اللقاحات بشكل أسرع : مزيج مثالي
سواء تمت صياغتها بطريقة تقليدية أو في نهج بيولوجيا الأنظمة ، تحتوي اللقاحات على مستضدات (شظايا بروتينية أو DNA) العامل الممرض (فيروسات أو بكتيريا أو طفيليات) ، والتي تؤدي إلى ردود فعل مناعية محددة للغاية. في بعض الأحيان تكون المستضدات فيروسات كاملة ومضعفة (مثل لقاح الجدري الذي طوره إدوارد جينر منذ 200 عام من صديد مستخلص من بثور الجدري لبقرة حلوب). في حالات أخرى ، تكون المستضدات عبارة عن شظايا من عامل مُعدٍ معطل (مثل لقاح شلل الأطفال Salk) ، أو جزيئات المستضدات وحدها تعمل كلقاح (على سبيل المثال ، لقاحات ضد الدفتيريا والسعال الديكي والكزاز). غالبًا ما تحتوي اللقاحات على مواد مساعدة – مواد تعزز الاستجابات المناعية. يستجيب الجهاز المناعي للمستضدات الموجودة في اللقاح في تسلسل محدد من الأحداث الجزيئية والخلوية التي تسمح للجسم بتجنب الإصابة في المستقبل بفيروس أو بكتيريا مع نفس أو مستضدات مماثلة. بالنسبة لمطوري اللقاحات ، فإن الهدف هو إيجاد مزيج من المستضدات والمواد المساعدة التي توفر الحماية الأكثر فعالية.
على الرغم من أنه تم تطويره بشكل تقليدي
على الرغم من أنه تم تطويره بشكل تقليدي ، إلا أن لقاح الحمى الصفراء YF- 17 D ، كان أحد أكثر اللقاحات فعالية على الإطلاق. تكفي حقنة واحدة ، ويتم حماية الموضوع بعد أسبوع واحد من الحقن ، وتستمر الحماية لمدة 30 عامًا على الأقل. مكّن هذا النجاح من اختبار مبادئ وأساليب بيولوجيا الأنظمة. تم إجراء دراسة بواسطة بالي بوليندران وفريق رافي أحمد من جامعة إيموري في أتلانتا ، وفريقي من معهد بيولوجيا الأنظمة في سياتل. لقد حاولنا إنشاء ملف تعريف دقيق للتغيرات الجزيئية والخلوية لشرح فعالية هذا اللقاح. من هذا الملف الشخصي ، حاولنا تحديد سبب لقاحات فيروس نقص المناعة البشريةلا تحفز الاستجابة المناعية اللازمة للتغلب على العدوى.
إقرأ أيضا:مراحل التطور النفسي الاجتماعيبدأنا تجربتنا بتلقيح لقاح YF- 17 D في 25 متطوعًا سليمًا. ثم أخذنا عينات دم من هؤلاء الأشخاص في أوقات مختلفة: أثناء الحقن ، ثم بعد 1 و 3 و 7 و 21 يومًا بعد ذلك. تم وضع كل عينة دم في جهاز فحص آلي للتعرف على طبيعة الجينات المنشطة (على جميع مكونات الدم). لا تنتج الجينات البروتينات التي تحتاجها الخلية مباشرة. يتم نسخ تسلسل الحمض النووي أولاً إلى رنا مرسال والذي بدوره يستخدم لتطوير البروتين. وهكذا ، من خلال فحص تركيزات ARN، نحدد الجينات التي تم تنشيطها وكذلك مستوى التعبير عنها.
تصميم اللقاحات بشكل أسرع : أدى تلقيح لقاح YF- 17 D أولاً إلى تنشيط الجهاز المناعي الفطري
كما هو متوقع ، أدى تلقيح لقاح YF- 17 D أولاً إلى تنشيط الجهاز المناعي الفطري ، وهو أول نظامي الدفاع في الجسم. يهاجم الجهاز المناعي الفطري على الفور مسببات الأمراض ، ويبتلعها ويقتل معظمها. على الرغم من أن النظام الفطري والسريع ولكن غير المحدد غالبًا ما يوفر دفاعًا فوريًا من تلقاء نفسه ضد التهديدات الخارجية ، إلا أنه يساعده نظام دفاع آخر ، وهو نظام المناعة التكيفي ، والذي ينتج استجابة محددة لمسببات الأمراض المعنية. هذه الاستجابة هي أن هناك ضررًا ضئيلًا أو معدومًا إذا واجه الموضوع نفس العامل المعدي مرة أخرى (انظر الإطار أعلاه) .
عن عشرة أيام بعد التلقيح، والدفاعات الفطرية من المتطوعين تلقيح مع YF- 17 إلى عززت نظام المناعة على التكيف، وتسبب إجابة جزئين. تم إنتاج الأجسام المضادة (بروتينات خاصة بأجزاء من فيروس الحمى الصفراء) أولاً ، ثم ظهرت مجموعة أخرى من الخلايا المناعية ، وهي الخلايا التائية السامة للخلايا ، والتي تحدد الخلايا المصابة وتدمرها. لقد حددنا 65 جينة تلعب دورًا رئيسيًا في استجابة الجسم للقاح YF- 17 D . يكشف تسلسل التعبير عن هذه الجينات عن تنشيط قوي للجينات التي تشفر الأجسام المضادة والخلايا اللمفاوية التائية السامة للخلايا.
وهكذا ، قمنا بالتحقق من صحة فرضيتنا: يمكننا تحديد الجينات التي تشفر مختلف اللاعبين في الجهاز المناعي والتي تم تنشيطها أو لم يتم تنشيطها بواسطة لقاح الحمى الصفراء. بشكل مستقل ، وجد رفيق بيير سيكالي ، من معهد فلوريدا للتلقيح والعلاج الجيني ، نتائج مماثلة.
ردود الفعل المناعية التي تم إطلاقها في موقع التطعيم فعالة
إن حقيقة أنه يمكننا “قراءة” في الدم ما إذا كانت ردود الفعل المناعية التي تم إطلاقها في موقع التطعيم فعالة ، ستجعل من الممكن تطوير اختبار تشخيصي بسيط: عن طريق سحب الدم عن طريق وخز بسيط في نهاية الإصبع ، يمكننا أن نعرف بسرعة ما إذا كان اللقاح فعالاً. لجمع وتحليل مثل هذه العينات ، لن يكون من الضروري استدعاء موظفين مؤهلين تأهيلا عاليا أو معدات باهظة الثمن. هذه نقطة مهمة عندما نعلم أن فيروس نقص المناعة البشرية والملاريا والسل تصيب بشكل أساسي أفقر مناطق العالم.
بعد أن أظهرنا أن بيولوجيا الأنظمة يمكن أن تعطي صورة دقيقة لتأثير اللقاح على جهاز المناعة ، عالجنا المشكلة التي يطرحها فيروس نقص المناعة البشرية . أردنا مقارنة العديد من تركيبات اللقاح ، لمعرفة ما إذا كان أي منها سيؤدي إلى استجابة مناعية “مثالية”. إلا أننا لا نعرف – وما زلنا لا نعرف – كيف تبدو الاستجابة المناعية المثالية في حالة فيروس نقص المناعة البشرية . هذا هو أحد أهدافنا الرئيسية اليوم. بدأنا بالبحث عن أدلة في الحيوانات.
تصميم اللقاحات بشكل أسرع : بحثًا عن المظهر المناعي المثالي
بعض القرود يمكن أن يصاب بفيروس نقص المناعة القردي ( فيما ) التي لديها .العديد من أوجه التشابه مع فيروس نقص المناعة البشرية . يقوم الآن لويس بيكر من كلية أوريغون للطب والعلوم ، وروبرت سيدر من المعهد الأمريكي للصحة ، وعلماء الأحياء في معهد سياتل بيوميد باختبار لقاحات مختلفة تحتوي على مستضدات لولبية لتوضيح .المظهر المناعي الذي يميز الاستجابة الفعالة. وبالتالي ، حددنا العديد من خصائص الاستجابة المناعية الفطرية التي .تجعل من الممكن التنبؤ باللقاحات التي ستحد بشكل أكثر فعالية من كمية الفيروس في دم الحيوانات المعرضة للبراغي .
تظهر الجينات المعنية
تظهر الجينات المعنية ، التي يرتبط تعبيرها بقدرة أفضل على محاربة الفيروس ،. كعقد لشبكة مكونة من جميع اللاعبين في الاستجابة المناعية ؛ تمثل كل عقدة جينًا وتشير الروابط بينها إلى التأثير الذي تمارسه .على بعضها البعض. نظرًا لوجود عدد كبير من الجينات المشتركة بين القرود والبشر ، يمكن أن يخبرنا ملف الاستجابة المناعية المثالية .للقرد عن ملف استجابة فيروس نقص المناعة البشرية لدى البشر ، ويمكن استخدامه لتقييم اللقاحات المختلفة.
بيكر و R.-P. يستكشف Sékaly مسارًا قريبًا. إنهم يطبقون نهج الأنظمة البيولوجية .لتحديد السبب في أن اللقاحات التي تحتوي على أشكال مخففة من اللولب تحمي القرود بشكل فعال. لسوء الحظ، في حالة من فيروس نقص المناعة البشرية ، وذلك باستخدام فيروس ضعف أبعد ما يكون خطيرا جدا. بمرور الوقت ، يمكن أن يتحد مع الأشكال .النشطة للفيروس ويجعل الأشخاص الذين كان من المفترض أن يحميهم مرضى (ولهذا السبب تم التخلي عن الشكل الحي الموهن لفيروس. شلل الأطفال في العديد من البلدان). إذا نجح هذا النهج ، فسنعرف كيفية إثارة استجابة مناعية مماثلة لتلك التي ينتجها فيروس موهن دون المخاطرة باستخدامه في اللقاح.
أكد علماء الأحياء الآن أن نهج “الأنظمة” يمكن أن يكون مفيدًا في تطوير اللقاح. لقد حصلنا على التوقيع المناعي المقابل للقاح فعال ( YF- 17 D ) والتوقيعات المناعية للقرود التي تم تحصينها بنجاح. ومع ذلك ، لا تزال هناك بعض الأشياء المجهولة التي يتعين إزالتها قبل تجربة لقاح جديد ضد فيروس نقص المناعة البشرية . كيف نفسر ، على سبيل المثال ، فشل لقاح معامل ميرك في عام 2007 ، والتي بدت مع ذلك واعدة؟